 普罗布考是一款兼具降脂与强效抗氧化功能的经典药物。近年来,其在神经系统保护领域的研究日益深入,而抗氧化正是其发挥神经保护作用的核心引擎。本次内容从分子层面解析普罗布考的抗氧化密码——从独特的酚羟基结构到直接激活谷胱甘肽过氧化物酶1(GPx1)的新机制。
普罗布考是一款兼具降脂与强效抗氧化功能的经典药物。近年来,其在神经系统保护领域的研究日益深入,而抗氧化正是其发挥神经保护作用的核心引擎。本次内容从分子层面解析普罗布考的抗氧化密码——从独特的酚羟基结构到直接激活谷胱甘肽过氧化物酶1(GPx1)的新机制。
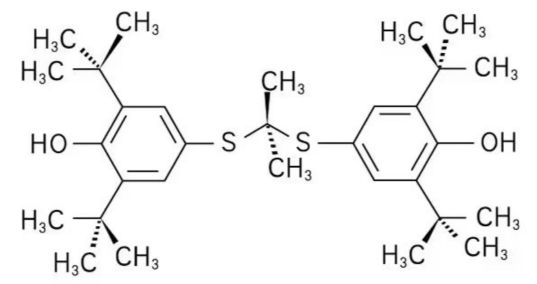
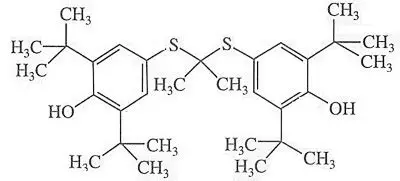
普罗布考分子式
酚羟基:抗氧化活性的结构基础
普罗布考分子中含有两个对称的酚羟基,易被氧化形成稳定的酚氧自由基,从而高效淬灭氧自由基、阻断脂质过氧化链式反应。这一结构特性使其不仅直接清除自由基,还能抑制低密度脂蛋白(LDL)的氧化修饰,从源头减少氧化应激损伤。与维生素E等经典抗氧化剂相比,普罗布考亲脂性更强,更易穿透生物膜及血脑屏障,在中枢神经系统内蓄积并持续发挥作用。
直接激活GPx1:一种全新的作用方式
2020年,Santos等发表Molecular Neurobiology的研究首次揭示:普罗布考可直接激活GPx1的酶活性,而不依赖其蛋白表达水平的上调。GPx1是细胞内主要的过氧化物分解酶,能将过氧化氢还原为水,从而保护神经元免受氧化损伤。该研究通过分子对接及酶动力学实验证实,普罗布考与GPx1活性位点特异性结合,增强其对过氧化物的亲和力。这一发现为普罗布考提供了全新的分子靶点,也为神经退行性疾病的抗氧化治疗开辟了新思路。
Nrf2通路:特定疾病模型中的保护证据
近年来,多项研究报道普罗布考可在部分神经系统疾病模型中调节核因子E2相关因子2(Nrf2)信号通路。
在坐骨神经慢性压迫性损伤诱导的神经性疼痛大鼠模型中,普罗布考通过增强Nrf2活性,上调下游抗氧化酶(如HO-1、NQO-1),从而减轻氧化应激及神经元损伤。
在脊髓损伤模型中,普罗布考可激活Nrf2/ARE信号通路,抑制炎症反应及神经元凋亡,促进神经功能恢复(Zhou等,2017)。
在糖尿病视网膜病变模型中,普罗布考通过上调Nrf2表达,减轻高糖诱导的视网膜神经元变性(Liu等,2020)。
上述研究提示,普罗布考对Nrf2通路的调控呈现疾病及组织特异性,其在不同病理条件下的激活机制尚需进一步探索。
小结
普罗布考的抗氧化机制是多层次、多靶点的:①直接清除自由基;②直接激活GPx1酶活性;③在特定神经损伤模型中调节Nrf2信号通路;④抑制LDL氧化及炎症信号通路。这些机制共同构成了其在中枢及周围神经系统中广泛保护作用的分子基础。深入理解这一“抗氧化密码”,将有助于临床更精准地定位普罗布考的获益人群,并推动其在新适应证中的探索应用。
参考文献:
【1】Santos, Dirleise Colle, Eduardo L G Moreira,et al. Probucol protects neuronal cells against peroxideinduceddamage and directly activates glutathione peroxidase-1[J]. Mol Neurobiol, 2020, 57(8): 3245-3257.
【2】Jin-Lan Huang, Chao Yu, Min Su, et al. Probucol,a "non-statin" cholesterol-lowering drug, amelioratesD-galactose induced cognitive deficits by alleviating oxidative stress via Keap1/Nrf2 signaling pathway in mice[J. Aging( Albany NY), 2019, 11(19): 8542-8555.
【3】Heng-Wei Liu, Yong Luo, Yu-Fan Zhou, et al. Probucol prevents diabetes-induced retinal neuronal degeneration through upregulating Nrf2[J]. Biomed Res Int,2020,2020:3862509.
【4】Zipeng Zhou, Chang Liu, Shurui Chen, et al. Activation of the Nrf2/ARE signaling pathway by probucol contributes to inhibiting inflammation and neuronal apoptosis after spinal cord injury[J]. Oncotarget,2017,8(32):52078-52093.